低温保存是长期保存生物材料的有效手段。目前,慢速冷冻与玻璃化方法已成功用于从细胞到部分组织的冻存。随着临床医学的快速发展,再生医学与器官移植对“即用型”大尺度组织或器官的保存需求急剧上升。对于结构复杂的大样本,玻璃化冻存较之传统慢速冷冻更具优势——它通过快速降温与复温,避免冰晶形成及其造成的机械损伤。理想情况下,玻璃化要求整个样本内部热量传递既可能快又尽量均匀,以防冰晶损伤和热应力破坏。然而,生物样本由于自身热阻高、导热差,如何在大尺度组织或器官中实现高效传热、避免致命性热应力损伤,长期以来始终是低温生物及临床医学领域面临的重大技术挑战和亟需解决的核心难题。
近日,中国科学院理化技术研究所低温科学与技术全国重点实验室液态金属与低温生物医学研究中心饶伟研究员与刘静研究员带领的团队在复杂器官深低温保存领域取得关键突破。他们开创性地提出了一种基于液态金属保护剂实现多尺度强化传热的器官低温保存范式,以其全新的“介入式”策略,成功打破了已有方法的理论与技术瓶颈。通过可组织注射、可血管网络灌注以及可在组织表面涂敷的新概念型液态金属保护剂,显著降低了遍布组织与器官的界面与接触热阻,并大幅提升了复温速率。新方法在组织和器官中构建了一条“热高速公路”,实现了快速均匀的热量传递,使热应力降低了两个数量级。在长达近10年的持续探索实践中,团队围绕兔皮肤、动脉和肾脏等多种尺度生物样本系统验证了新方法的有效性。尤为重要的是,该技术在国际上首次实现了玻璃化冻存10mL级兔肾脏一周后的成功同种异体移植,并支持受体动物存活。这一突破为复杂组织与器官的保形冻存提供了普适、多尺度强化降温与复温策略,为突破器官救治的“时间与空间极限”提供了颠覆性冻存取用途径,有望缓解供体器官严重短缺问题,进而革新挽救生命的移植手术。
深低温玻璃化保存(-120℃~-196℃)是突破现有器官短期保存局限(通常仅数小时至数天)的理想方案,有望实现器官的长期甚至永久性储存。然而,真实器官具有复杂的多层级血管网络和异质异构特征,且生物组织自身的热导率极低。在实现玻璃化所需的极快速降温和复温过程中,器官内部与表面极易产生巨大的温度梯度。这种非稳态传热不仅会导致不可控的冰晶生成刺破细胞,更会引发巨大的热应力,导致器官发生宏观的“热碎裂”,造成不可逆的低温损伤。传统单纯依靠外部金属箔包裹或灌注磁性纳米颗粒的传热方式,由于存在界面接触热阻大、内部热源分布不均等问题,始终难以逾越这一传热“天堑”。
长期以来,研究团队瞄准这一重大科学与技术难题,开启了器官深低温保存的探索之路。研究团队创造性地提出以镓基液态金属作为高性能传热介质,构建了全新的介入式强化传热理论与技术。团队自主研发了一种由镓铟合金与聚乙烯吡咯烷酮(PVP)混合而成的柔性液态金属低温保护剂(LMP)。该材料导热系数高达9.3 W/m·K,比传统纳米复温液提升了近10倍,为目前已报道冷冻保护介质中的最高值。基于此,团队提出了一种全新理念的“介入式强化传热”策略(图1):(1)利用液态金属保护剂在低温下的相变平整化特性,使其如同“液态铠甲”般完美、紧密地贴合在不规则器官表面,大幅降低了传统刚性金属材料难以避免的接触热阻与界面热阻(图2);(2)将液态金属随保护剂灌注进入器官复杂的血管网络,利用其优异的电磁热效应,在交变磁场下实现由内而外的均匀体积加热。这种“表面+体积”的跨尺度协同强化传热新范式,彻底打通了器官内外的传热路径。同时值得指出的是,该方法借助明胶材料作为过渡层,还实现了液态金属高导热保护材料的快速洗脱及高效回收,大大提升了新方法的生物安全性和临床转化潜力。
研究团队在多尺度生物组织和器官上系统验证了该技术的有效性。在皮肤与血管玻璃化保存(-196℃)实验中,介入式强化传热(IHT)技术将皮肤(图3)和血管组织(图4)复温后的存活率分别提升了1.7倍和3.6倍,且移植后的皮肤表现出更强的自我愈合能力。更为令人瞩目的是,研究还挑战了具有高度复杂结构的10mL级中等模式动物器官——兔肾脏的深低温保存。实验表明,在IHT技术的加持下,降温和复温过程中肾脏的最大表面温差大幅降低了10~41.9℃,热应力被显著降低了两个数量级,成功实现了快速、均匀的冷却与复温,完美避免了器官的热碎裂。经过长达7天的-150℃深低温玻璃化保存后,复温后的兔肾脏不仅保持了完好的宏观形态与微观组织结构,更重要的是,团队成功将这些经过深低温保存的肾脏进行了同种异体移植(Allogeneic transplantation)。术后监测显示(图5),移植肾脏迅速恢复了血流灌注,形态结构保持完整,并在受体兔体内成功实现了生命支持(100%存活,生存期≥4天),血液生化指标及尿液分析均显示肾功能得到有效恢复,这一成效在以往的文献中尚未被报道过。
从全球进展来看,此前领域内的突破性成果局限于小尺度大鼠肾脏(~1ml)的玻璃化冻存和异体移植验证,而针对体积约10ml的兔肾脏模型,目前仅有研究报道了自体移植且存活率仅1/3的个例。与以上国际进展相比,理化所研究团队此次实现了10ml兔肾脏玻璃化保存复温后器官异体移植尺度的跨越(1ml→10ml),建立了较为完整的材料学、工程热物理、器官灌注仪器平台、低温损伤及生物学评估全流程方法(图5),彰显了新技术在大尺度器官深低温保存与移植中的临床应用潜力。
相关研究以Liquid metal cryoprotectants for scalable biosamples cryopreservation为题发表于Cell出版社旗下期刊Matter,为规模化器官库构建、临床器官移植发展提供了基础理论和技术支撑,有望发展成一种通用型高性能低温保存方法(图6)。论文第一作者为理化所特别研究助理后仪博士和汪晓红博士,通讯作者为饶伟研究员和刘静研究员。
未来,液态金属低温保护剂及介入强化冻存与复温技术可进一步拓展至人体尺度器官(如肾脏、肝脏、心脏等)的长期低温保存中,从而为器官移植、组织工程与再生医学带来变革性发展契机。本研究得到了低温科学与技术全国重点实验室的大力支持,并受到中国科学院战略性先导科技专项、国家自然科学基金、中国科学院理化技术研究所所长基金、中国博士后科学基金会项目等资助。
原文链接:
Liquid metal cryoprotectants for scalable biosamples cryopreservation
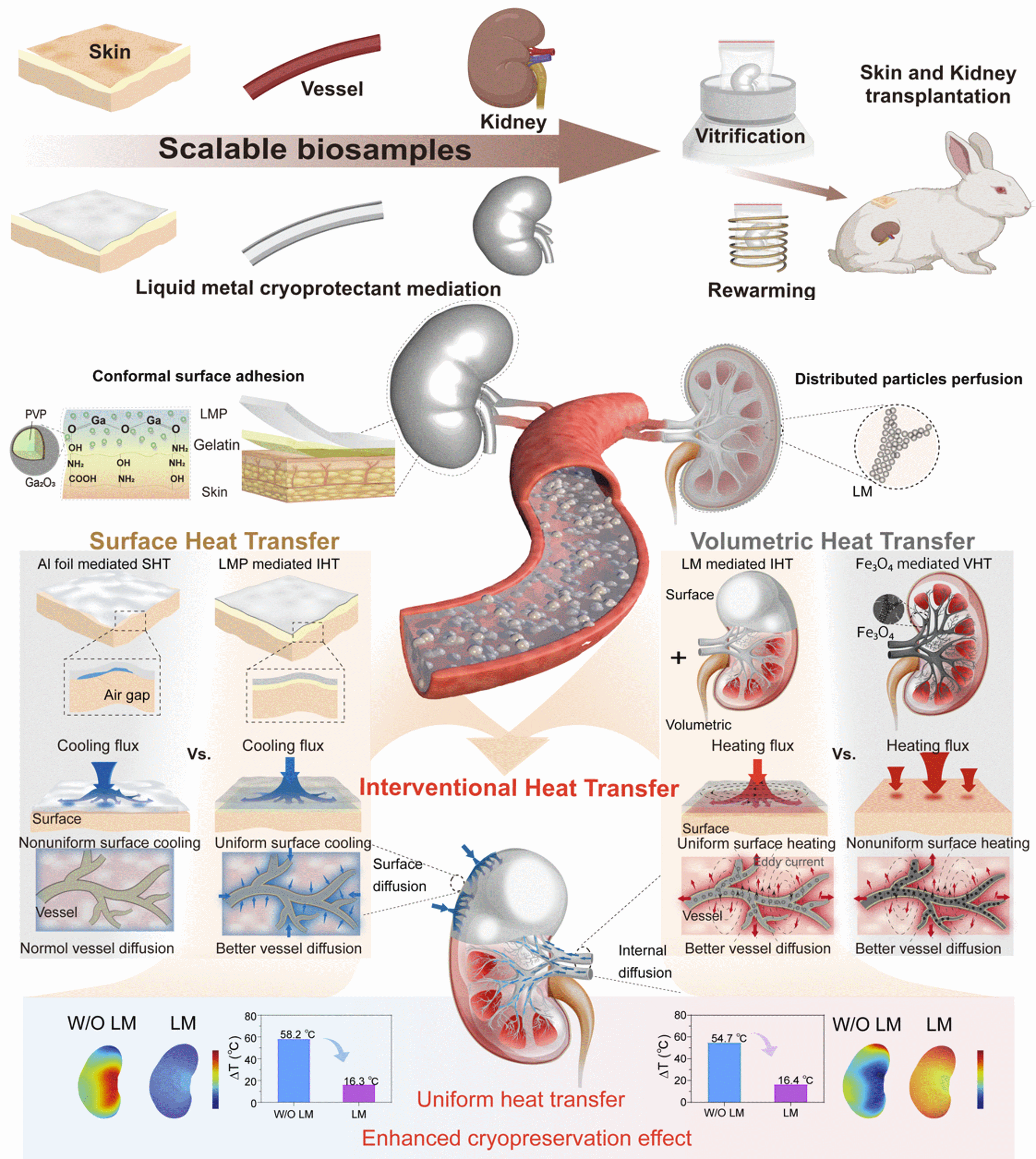
图1. 基于液态金属低温保护剂及多尺度介入强化传热的器官低温保存方法
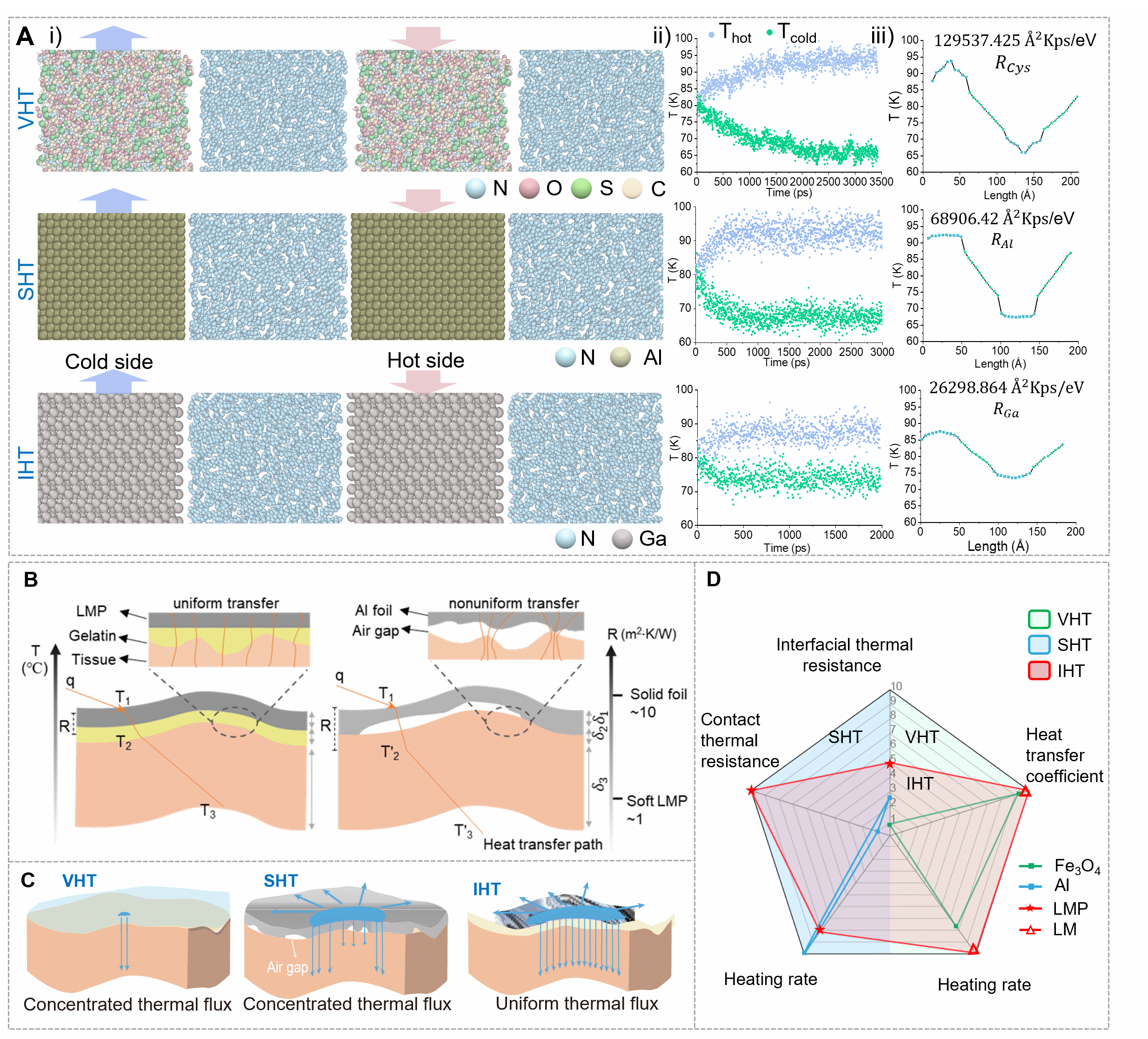
图2. 液态金属介入强化传热。(A) 降低界面热阻;(B) 降低接触热阻;(C) 提升热扩散性能;(D) 综合热性能雷达图
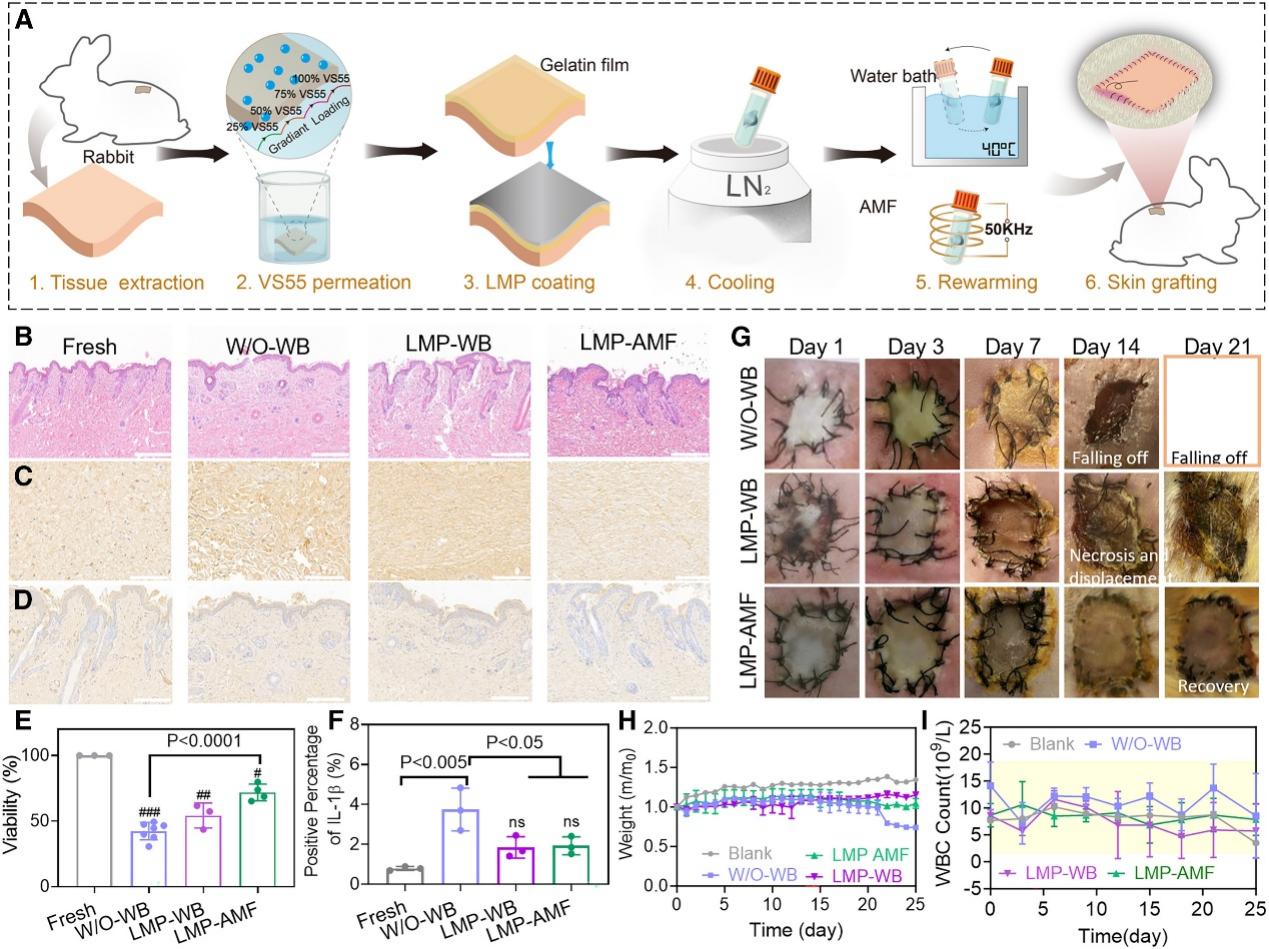
图3. 基于液态金属介入强化传热的皮肤低温保存与移植试验情况
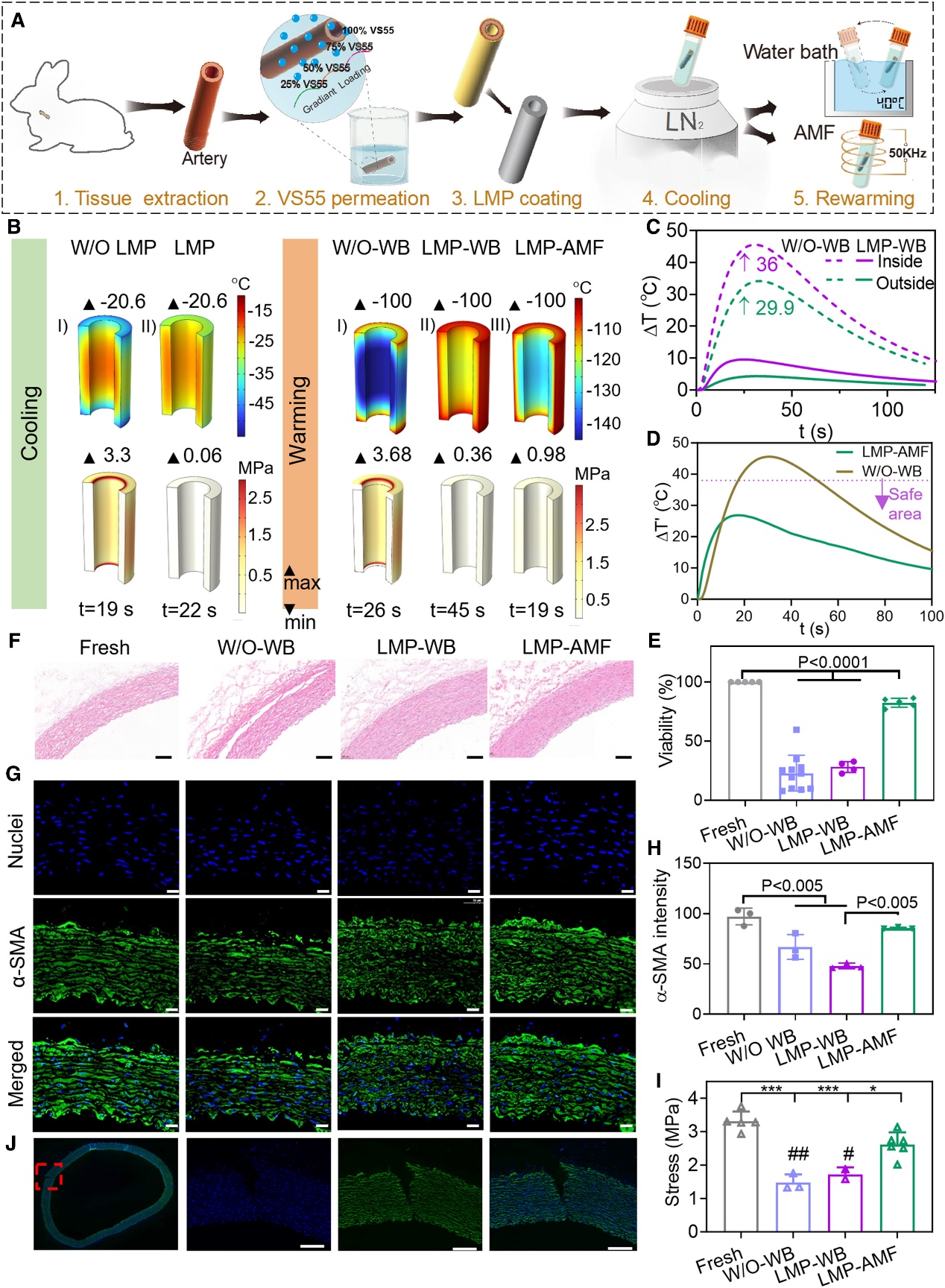
图4. 基于液态金属介入强化传热的血管适形化低温保存
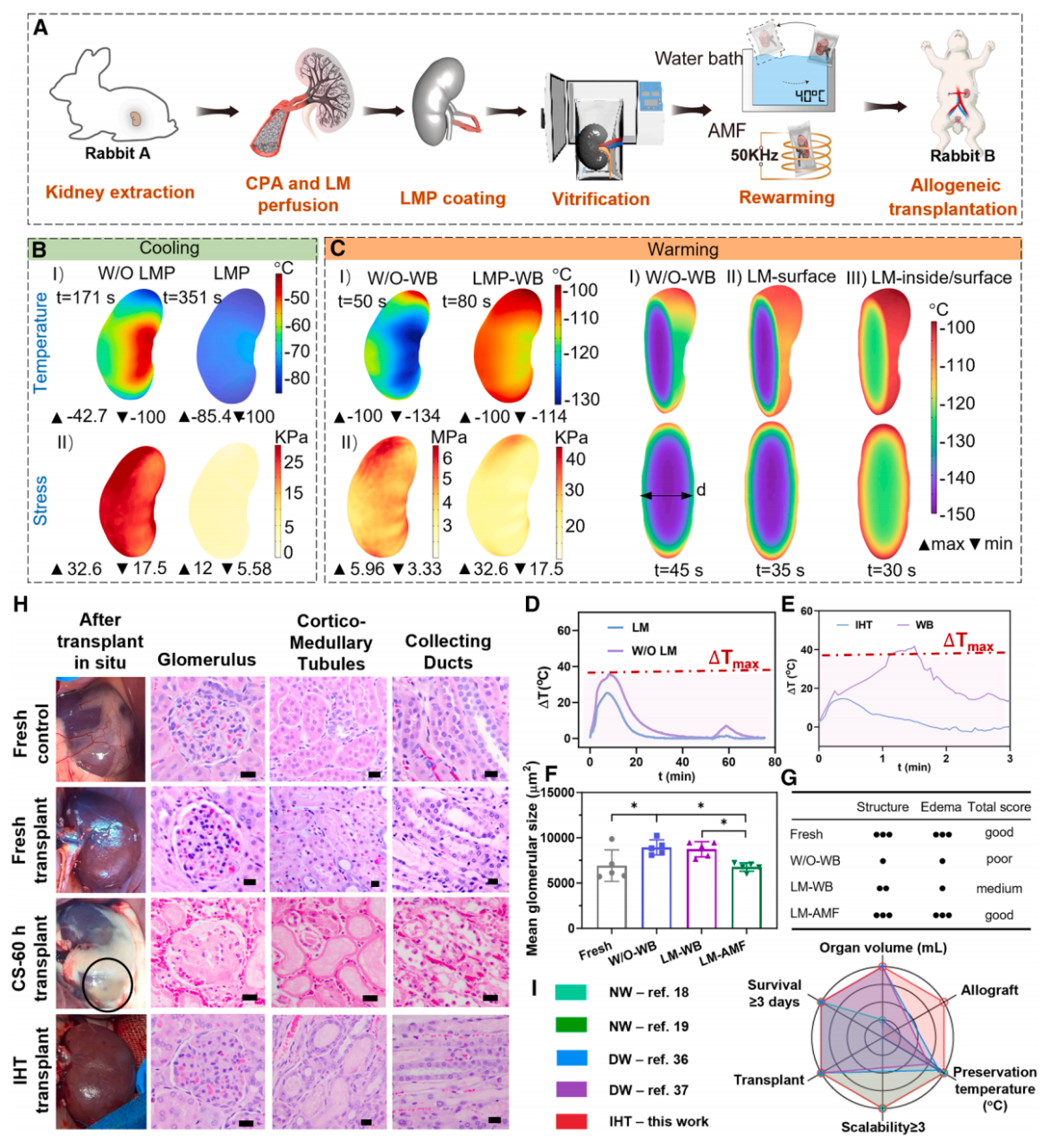
图5. 兔肾脏玻璃化保存和异体移植受体动物功能评估

图6. 基于液态金属低温保护剂及介入强化传热方法的兔肾脏玻璃化保存全流程示意
新闻中心